BIOBADASAR FASE III es el registro de acontecimientos adversos y seguridad en tratamientos biológicos, pequeñas moléculas y biosimilares de la Sociedad Argentina de Reumatología, que se lleva adelante en colaboración con el BIOBADASER de la Sociedad Española de Reumatología. Se trata de un estudio prospectivo de casos y controles en el cual se incluyen pacientes con enfermedades reumáticas inflamatorias (listado en ANEXO 1) en tratamiento con drogas biológicas o pequeñas moléculas (casos) (listado en ANEXO 2), y pacientes con DMARDs convencionales (controles). El registro entró en funcionamiento en agosto de 2010 y a la fecha cuenta con más de 5500 pacientes en seguimiento en 54 centros distintos de todo el país.
El objetivo del registro es evaluar la seguridad de estos fármacos a largo plazo y en la vida real, logrando poner en evidencia incluso los eventos infrecuentes. A su vez, BIOBADASAR permite conocer datos de la vida real sobre el uso, sobrevida y motivos de discontinuación de las terapias dirigidas gracias al registro de los índices de actividad de las enfermedades.
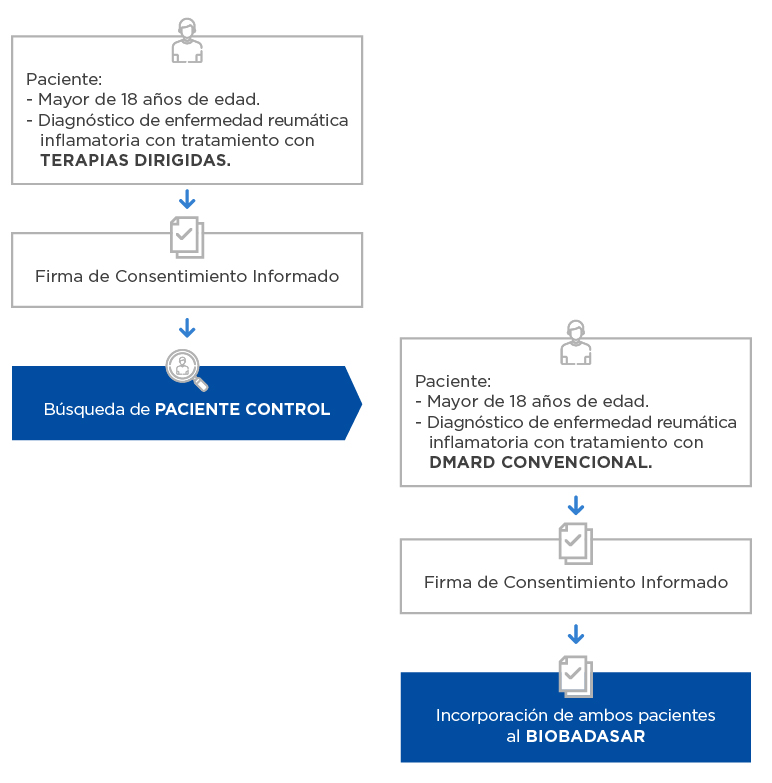
BIOBADASAR es un registro nacional, multicéntrico, prospectivo y observacional en el que se incluye a aquellos pacientes con diagnóstico de enfermedad reumática inflamatoria y tratamiento con terapias dirigidas (casos) o con DMARDs convencionales (controles). Aquellos pacientes que requieren cambiar de tratamiento convencional a terapias dirigidas pueden permanecer en el registro pero su estatus cambia a “caso” y se requiere la inclusión de 2 nuevos controles. Los pacientes son seguidos hasta el retiro del consentimiento, pérdida de seguimiento en el centro o muerte.
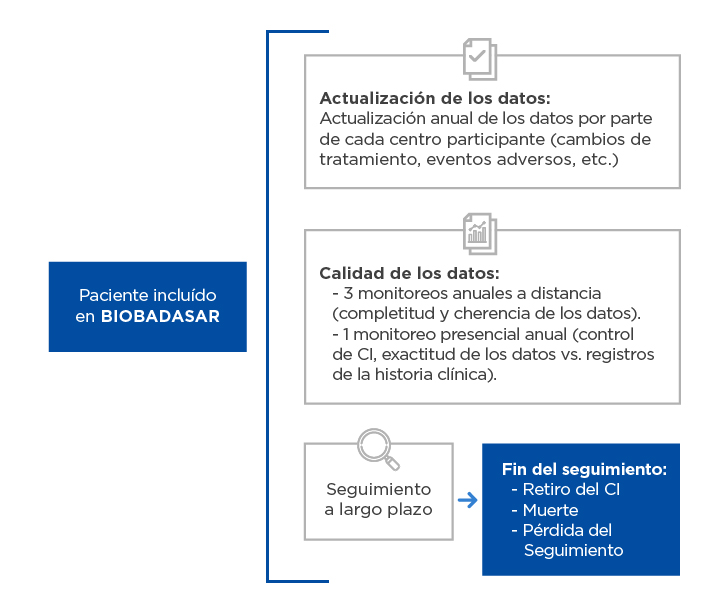
Para garantizar la calidad de los datos, todos los centros se comprometen a actualizar al menos una vez al año todos los datos de sus pacientes, y se someten anualmente a 3 evaluaciones a distancia y 1 evaluación presencial por parte de los monitores del estudio.
El registro BIOBADASAR 3.0 se ha consolidado como una herramienta clave en el monitoreo y análisis de la seguridad y efectividad de las drogas biológicas y pequeñas moléculas en el tratamiento de enfermedades reumáticas en nuestro país. Con 15 años de recolección continua de datos, ha generado conocimiento invaluable sobre el uso de estos tratamientos en la práctica clínica real, adaptado a las necesidades y características de nuestra población.
A nivel internacional, BIOBADASAR 3.0 ha colaborado en la conformación de BIOBADA-LATAM, una iniciativa conjunta con los registros de Brasil, México, Paraguay y Uruguay, que busca comprender el impacto de estos tratamientos en la región. Además, se destaca su colaboración con otras entidades internacionales incluyendo la Universidad de Leiden, con el fin de aportar datos al conocimiento global. Este esfuerzo sostenido es resultado del compromiso de profesionales de todo el país que participan activamente en el registro.
